
|
申请III类的Global Kinetics公司开发的移动医疗设备Personal KinetiGraph,可监测和治疗帕金森病,针对帕金森患者的活动提供全面的自动化报告,使神经科医生和其他医生可以更容易地识别运动症状的变化,帮助决策以优化治疗。
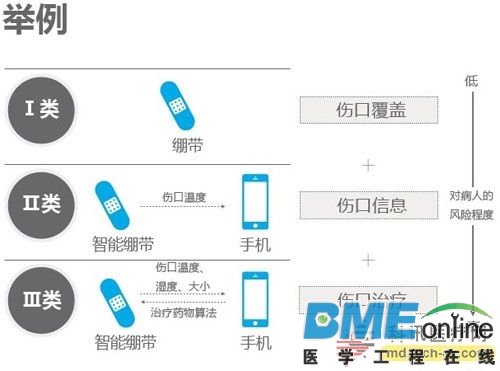
三类医疗设备的差别是?以绷带举例,普通绷带仅仅是覆盖伤口无其他作用,则归属Ⅰ类;与手机连接,能够通过应用查看伤口温度,且不小心还可能伤口感染,对会诊会有轻度风险,归属Ⅱ类;连接手机后,不只能显示伤口相关信息,还能通过药物算法给予患者反馈、指导等,归为Ⅲ类。
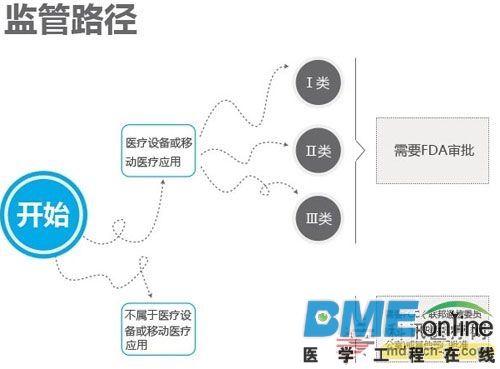
 确定你的产品后,然后结合合适的监管路径和商业模式.如果你的模式是收费,那么你就可能会需要发表临床结果及获得FDA批准。
 以下是动脉网就FDA对移动医疗(智能手机连接的医疗设备和独立应用程序(App))的审批情况做的数据整理。2014年度,迄今为止,FDA已批准了31个数字健康产品。
FDA审批通过的移动医疗项目集中在4个类别
今年通过FDA510(k)审核的移动医疗项目类别主要有app、软件工具、移动医疗设备、移动医疗设备app四个类别,除了软件工具稍少以外,其余类别不相上下,软件工具的项目细分领域主要是医生工具——移动影像业。
 |