
|
LeMaitre Vascular, Inc.对不透射线标记尺主动召回 乐脉医疗科技(上海)有限公司报告,由于标签错误,生产商LeMaitre Vascular, Inc.对不透射线标记尺(注册证编号:国械注进20152313815)主动召回。召回级别为三级。涉及产品的型号、规格及批次等详细信息见《医疗器械召回事件报告表》。 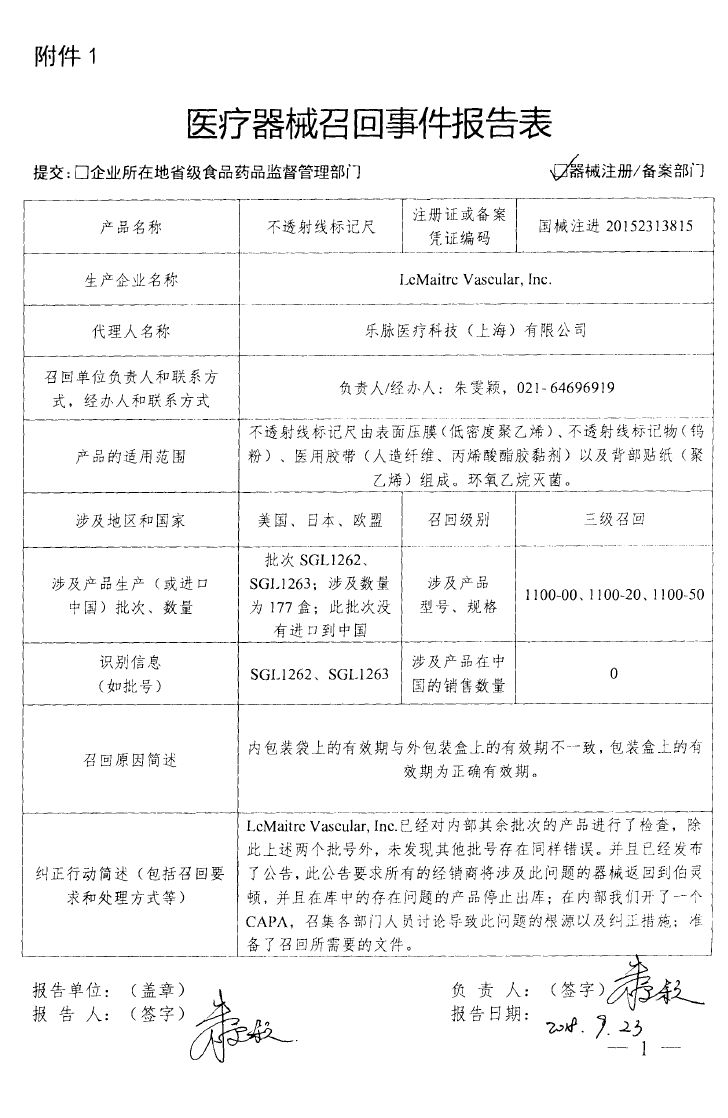 Merit Medical Systems,Inc对高压造影注射延长管主动召回 麦瑞通医疗器械(北京)有限公司报告,由于标签错误,生产商Merit Medical Systems,Inc对高压造影注射延长管(注册证编号:国械注进20163770745)主动召回。召回级别为三级。涉及产品的型号、规格及批次等详细信息见《医疗器械召回事件报告表》。 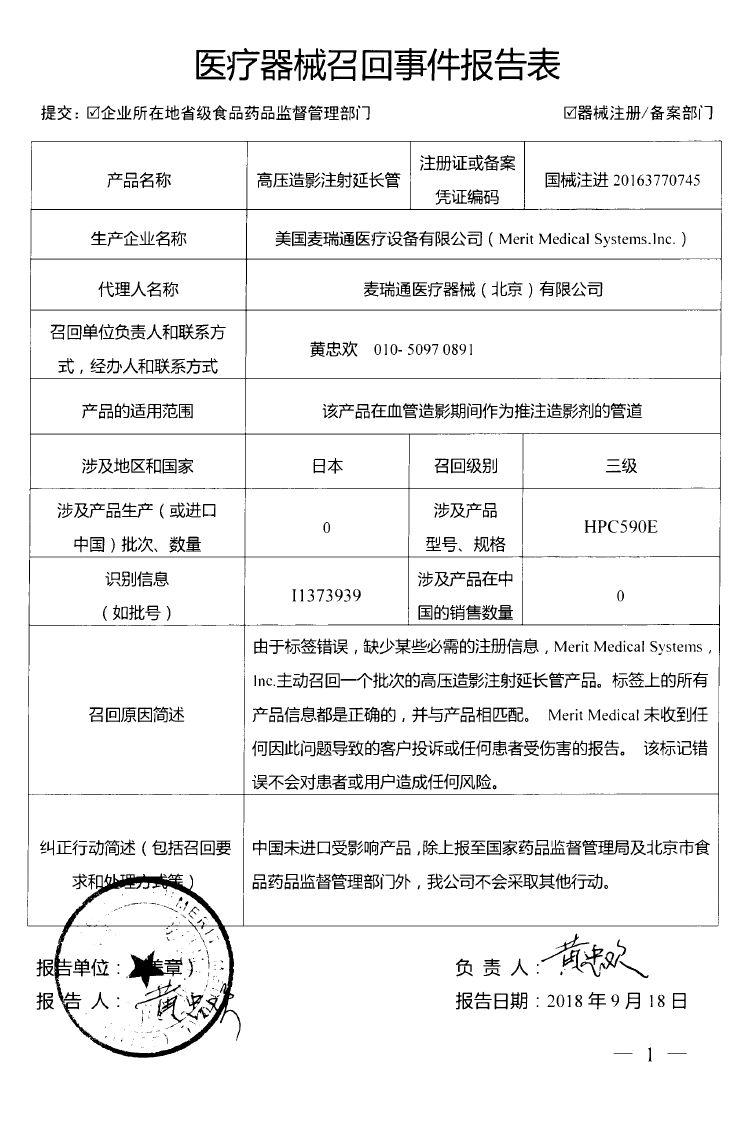 波科国际医疗贸易(上海)有限公司对植入式心脏再同步治疗起搏器、植入式心脏起搏器主动召回 波科国际医疗贸易(上海)有限公司报告,由于氢诱发而使电池耗竭加快将导致机器提前更换的可能性变高,波科国际医疗贸易(上海)有限公司对植入式心脏再同步治疗起搏器(注册证编号:国械注进20163212749、国械注进20163212837)植入式心脏起搏器(注册证编号:国械注进20163212750、国械注进20163212751、国械注进20163212842)主动召回。召回级别为二级。涉及产品的型号、规格及批次等详细信息见《医疗器械召回事件报告表》。 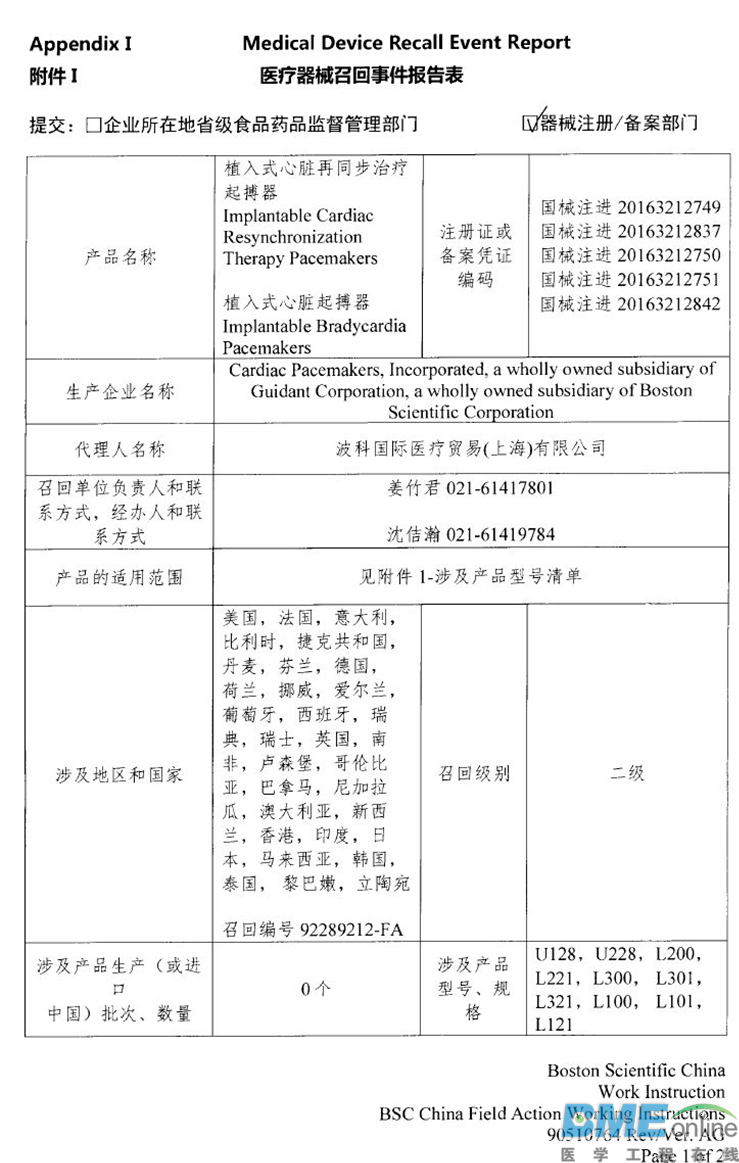  Biomet Orthopedics对临时股骨假体成型用一次性骨水泥模具主动召回 捷迈(上海)医疗国际贸易有限公司报告,由于涉及产品存在潜在的混批风险,生产商Biomet Orthopedics对临时股骨假体成型用一次性骨水泥模具(注册证编号:国械注进20163461466)主动召回。召回级别为二级。涉及产品的型号、规格及批次等详细信息见《医疗器械召回事件报告表》。 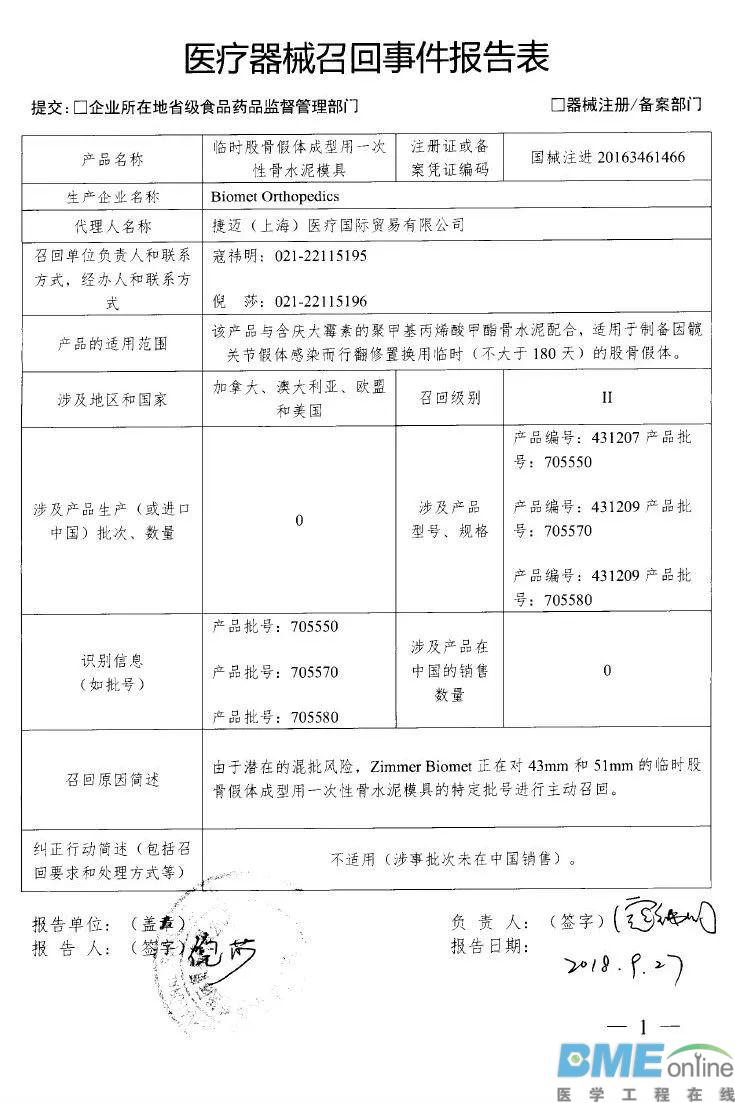 Bard Peripheral Vascular,Inc.对乳腺定位针(商品名:Ghiatas)主动召回 巴德医疗科技(上海)有限公司报告,由于涉及产品规格错误,生产商Bard Peripheral Vascular,Inc.对乳腺定位针(商品名:Ghiatas)〔国食药监械(进)字2014第3151392号〕主动召回。召回级别为三级。涉及产品的型号、规格及批次等详细信息见《医疗器械召回事件报告表》。   Philips Medical Systems对半自动体外除颤器主动召回 飞利浦(中国)投资有限公司报告,由于涉及产品可能不符合其IPx5防水性能规范,生产商Philips Medical Systems对半自动体外除颤器(注册证编号:国械注进20153213377)主动召回。召回级别为二级。涉及产品的型号、规格及批次等详细信息见《医疗器械召回事件报告表》。 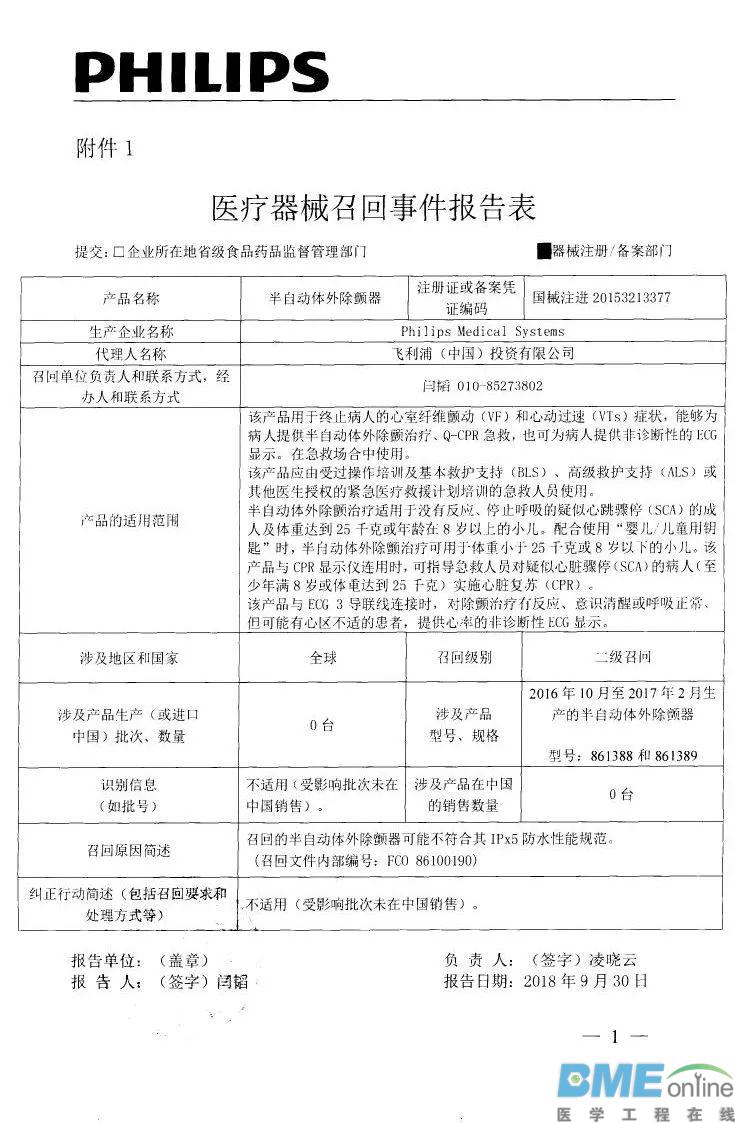 B.Braun Surgical SA对可吸收外科缝线主动召回 贝朗医疗(上海)国际贸易有限公司报告,由于涉及产品的包装有破损,生产商B.Braun Surgical SA对可吸收外科缝线(注册证编号:国械注进20173651559)主动召回。召回级别为二级。涉及产品的型号、规格及批次等详细信息见《医疗器械召回事件报告表》。 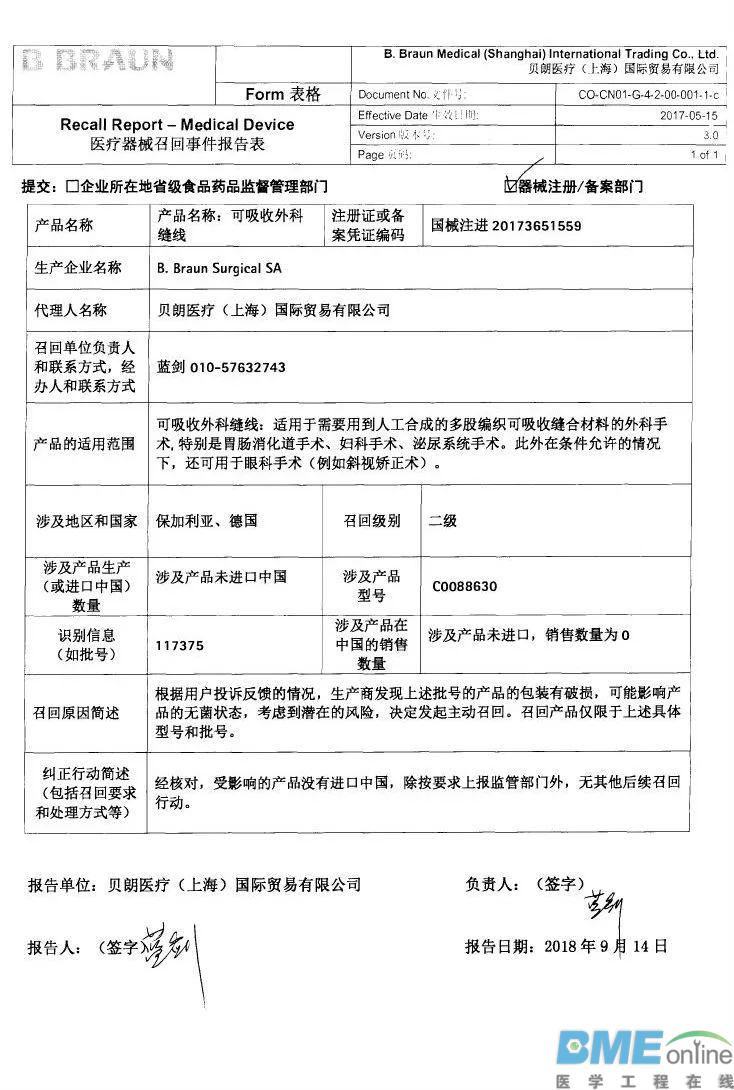 GE Healthcare对影像归档及传输系统、影像归档及传输软件主动召回 通用电气医疗系统贸易发展(上海)有限公司报告,由于发现部分批次产品在获取图像的进程中可能发生数据库处理问题,从而影响获取图像的完整性,生产商GE Healthcare对影像归档及传输系统〔国食药监械(进)字2014第2702186号〕、影像归档及传输软件〔国食药监械(进)字2014第2702186号、国械注进20182701756〕主动召回。召回级别为二级。涉及产品的型号、规格及批次等详细信息见《医疗器械召回事件报告表》。 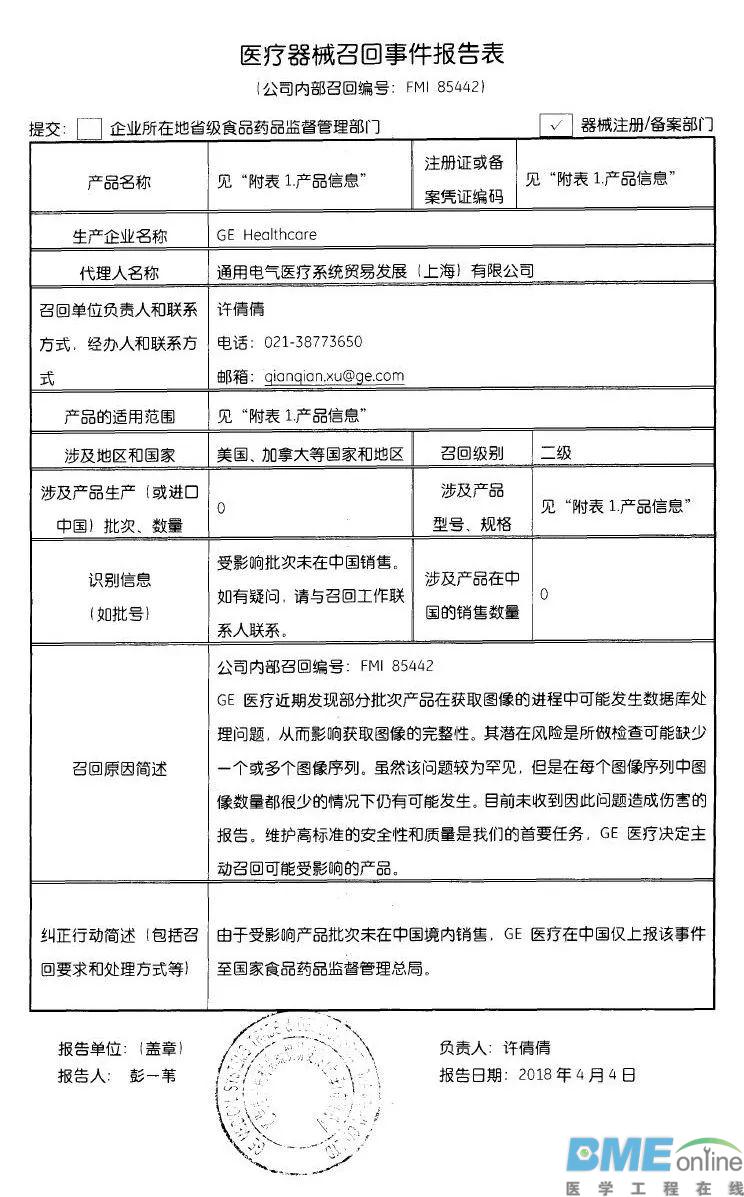 Smith & Nephew,Inc.对膝关节手术器械主动召回 施乐辉医用产品国际贸易(上海)有限公司报告,由于涉及产品远端截骨模块的扣环过薄导致无法与远端定位导板锁定,生产商Smith & Nephew,Inc.对膝关节手术器械(备案号:国械备20151696号)主动召回。召回级别为三级。涉及产品的型号、规格及批次等详细信息见《医疗器械召回事件报告表》。 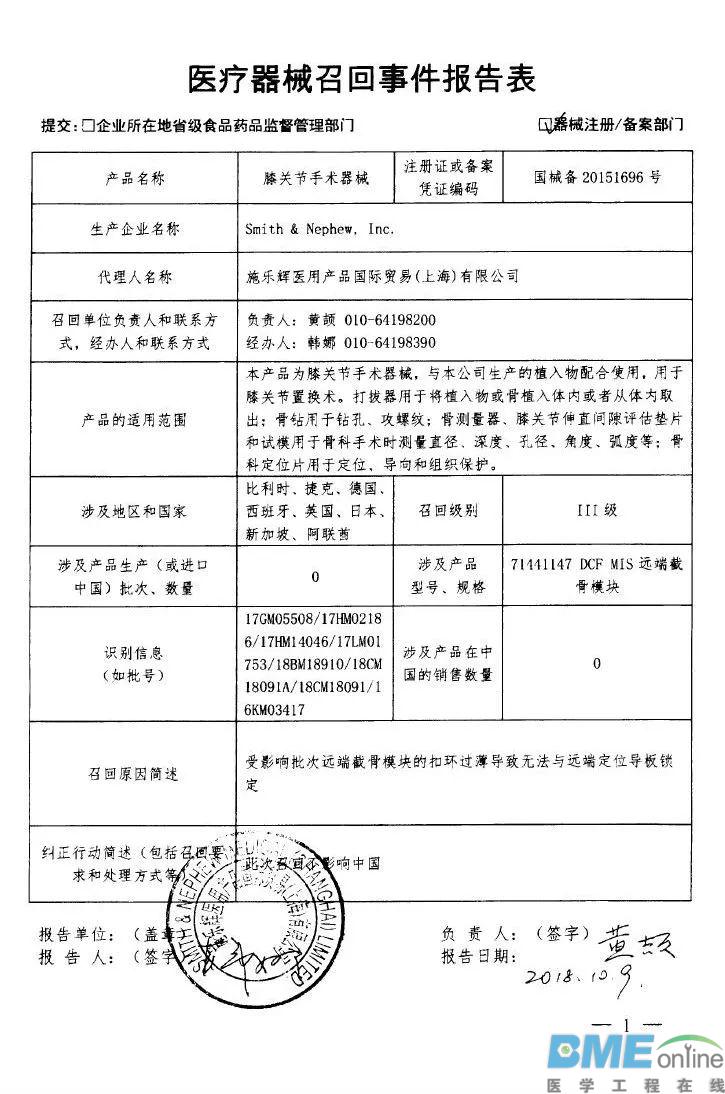 Ventana Medical Systems, Inc.和Roche Diagnostics GmbH对DAB染色液等产品变更召回级别 罗氏诊断产品(上海)有限公司报告,由于试剂分配器关键部位硅油不足,生产商Ventana Medical Systems, Inc.和Roche Diagnostics GmbH对DAB染色液等产品主动召回,相关产品召回信息已于2018年9月3日发布,召回级别为二级。现召回级别改为一级。涉及产品的名称、注册证或备案凭证编码、型号、规格及批次等详细信息见《医疗器械召回事件报告表》。  来源:NMPA
|